谷歌旗下、同样由DeepMind首席执行官Demis Hassabis领导的Isomorphic Labs,发布了一款被《自然》期刊称为“AlphaFold 4”的新一代AI药物设计引擎:IsoDDE。
它的性能全面超越前代,但这次,它选择了完全闭源。AI助力科学研究的黄金时代,那扇敞开的大门,似乎正在缓缓关闭。

回顾2024年,Demis Hassabis因AlphaFold站上了诺贝尔领奖台。这个能够精准预测蛋白质三维结构的AI模型,被190多个国家的超过300万名研究者使用,堪称AI普惠全人类的标杆。诺贝尔委员会嘉奖的,与其说是一个算法,不如说是一种精神——将最强大的科学工具免费交到每一位研究者手中。
仅仅16个月后,“AlphaFold”的继承者便已亮相。2026年2月10日,Hassabis创办的AI制药公司Isomorphic Labs发布了一份长达27页的技术报告,展示了一套名为IsoDDE的药物设计引擎。其性能全面碾压AlphaFold 3,被哥伦比亚大学的计算生物学家Mohammed AlQuraishi评价为“AlphaFold 4级别的重大进步”。

然而,这一次,情况截然不同。代码不会公开,论文不会发表,核心方法也不会共享。Isomorphic Labs总裁Max Jaderberg对《自然》的表述非常直白:“我们不打算公开‘秘方’。”

这或许意味着,AlphaFold的开源传奇,很可能到第三代就画上了句号。
性能提升显著,能力令人震撼
在讨论争议之前,我们有必要先了解IsoDDE究竟做到了什么,这有助于理解为何其“闭源”选择会引发如此大的波澜。
打一个不太严谨的比方:如果把蛋白质想象成一把锁,药物分子就是钥匙。此前AlphaFold的贡献,是帮我们无比清晰地“看清”了这把锁(蛋白质)长什么样。但这还远远不够——你还需要知道钥匙(药物)插进去后能不能转动、结合得紧不紧,甚至需要发现锁上是否还存在其他未被注意到的“钥匙孔”(隐藏结合位点)。
IsoDDE要回答的,正是这些更复杂、更贴近药物发现实际需求的问题。它是一个统一的预测引擎,将蛋白质结构预测、分子结合强度计算、隐藏结合位点发现等多种能力整合在了一起。
数据最能直观地说明其强大。
在一项专门考验AI模型处理“从未见过”的新颖蛋白结构能力的基准测试(Runs N' Poses)中,当测试样本与训练数据的相似度极低(0-20%,这是最困难的情况)时,IsoDDE的成功率达到了AlphaFold 3的两倍以上。
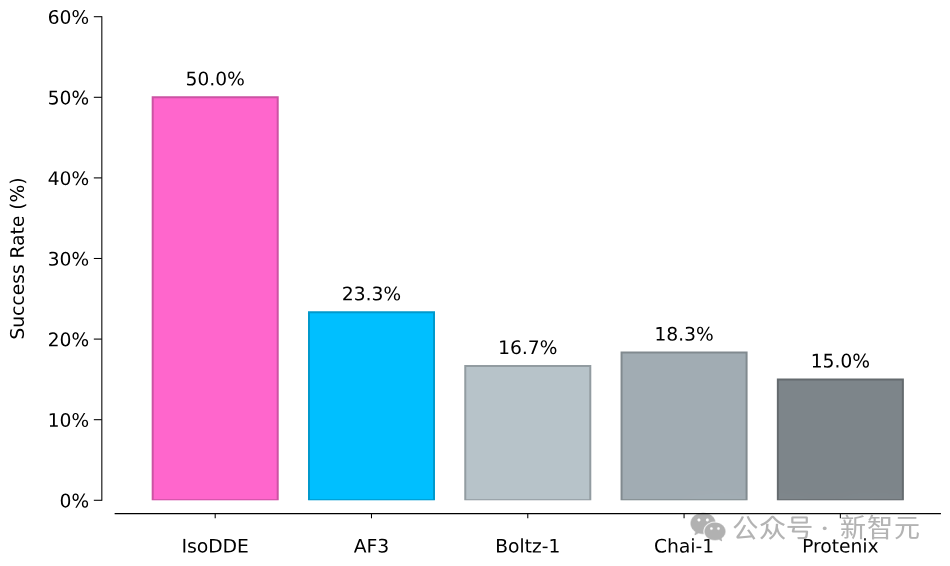
在60个最具挑战性的案例中,有17个是AlphaFold 3彻底失败而IsoDDE成功预测的。

在预测抗体如何识别其靶标这一任务上,IsoDDE的高精度预测成功率是AlphaFold 3的2.3倍,是另一个主流开源模型Boltz-2的近20倍。
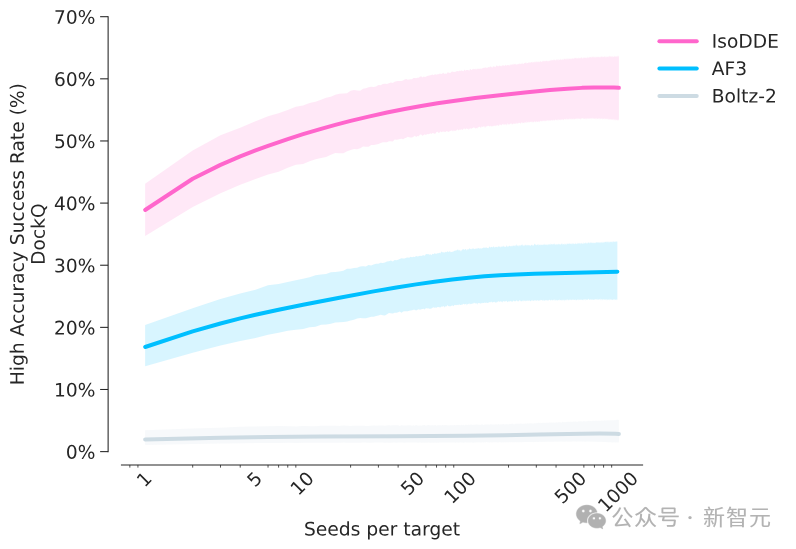
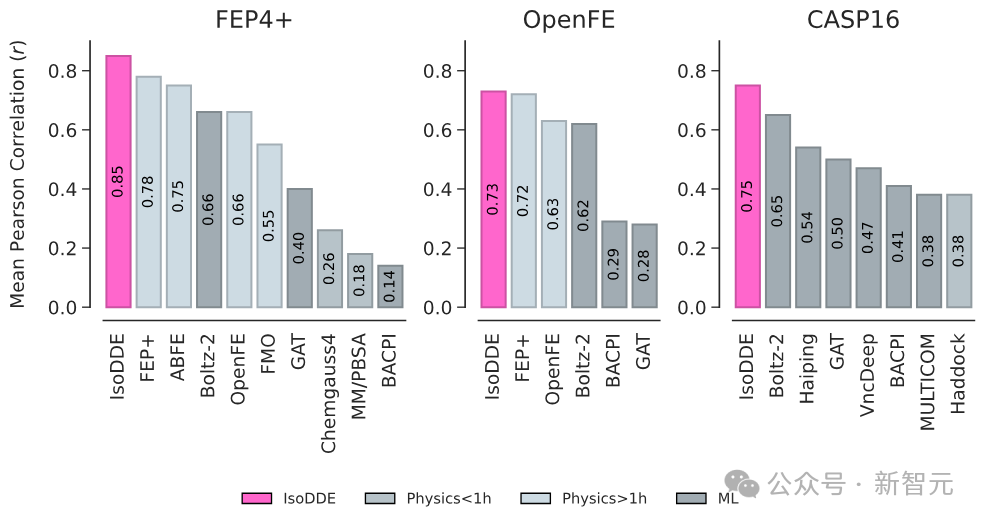
最令同行惊讶的,是其对结合亲和力(判断药物分子与靶点结合紧密程度)的预测能力。这项任务传统上严重依赖名为“自由能微扰”的物理模拟方法,计算成本极高,且通常需要实验测得的晶体结构作为起点。
而IsoDDE在多个公开测试中,不仅全面超越了所有AI方法,甚至超过了传统的物理模拟方法。关键在于,它完全不需要任何实验数据作为起点。
技术报告中还有一个非常引人注目的案例。一个名为cereblon的蛋白质,科学家们花了15年时间,一直以为它只有一个药物结合位点。直到2026年初,一篇新论文才通过实验发现了第二个隐藏的结合位点。而IsoDDE仅输入该蛋白的氨基酸序列,就在几秒钟内准确找出了这两个位点——包括那个隐藏了15年的。
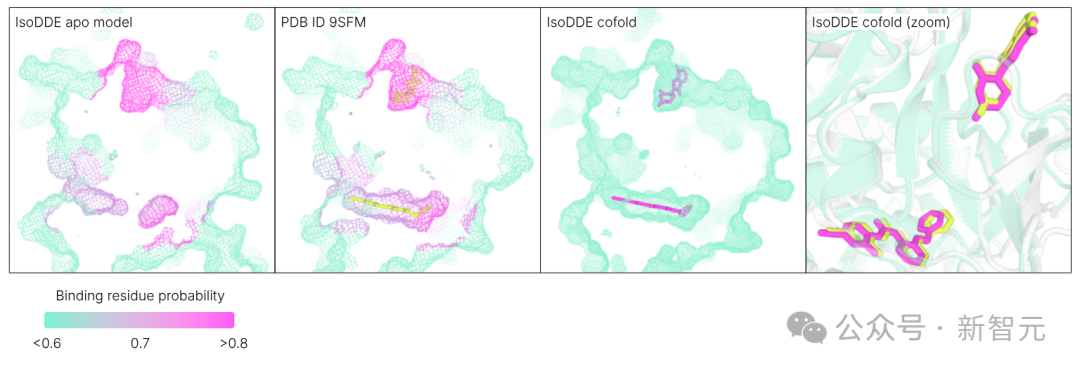
实验室要完成同样的发现,需要耗费大量时间和昂贵的晶体浸泡实验。IsoDDE的效率是颠覆性的。正如AlQuraishi所言,最令人震撼的是IsoDDE在完全陌生的分子体系上展现出的强大泛化能力,“这说明他们一定做了非常新颖的东西”。
闭源策略,引发学界忧虑
如果IsoDDE只是一个普通的商业软件,闭源是天经地义的。问题在于,它的“前辈”AlphaFold代表了一种截然不同的价值观。
AlphaFold 2在2021年开源,配套论文发表在《自然》上,其预测结果数据库免费向全球开放。这件事的意义远超技术本身——它证明了一种可能性:由科技巨头资助的最前沿AI研究,可以真正成为全人类共享的公共品。超过300万科学家利用它加速了自己的研究,无数项目因此受益,它切实改变了生物学研究的进程。

2024年发布的AlphaFold 3同样发表了详细的论文,虽然其代码开源的节奏曾引发一些争议,但最终仍面向学术界开放了权重。

IsoDDE打破了这个传统。长达27页的技术报告中,几乎没有透露任何关于模型架构和训练方法的关键细节。《自然》报道的副标题直截了当地指出:科学家们“只能猜测如何实现类似的结果”。

Jaderberg说,他希望这份报告能“激励”其他团队。但AlQuraishi的反应恐怕更能代表学术界的真实感受:“问题在于,我们对细节一无所知。”

当然,作为一家商业公司,Isomorphic Labs保护自己的核心技术合情合理。但值得深思的是:当AI在科学领域的能力越来越强大,且越来越集中于少数几家巨头公司手中时,这些能力的开放程度,应由谁来决定?
Isomorphic Labs已获得6亿美元融资,与礼来、诺华等制药巨头签署了潜在价值近300亿美元的合作协议,内部运行着17条药物研发管线。Hassabis本人也在2026年1月的达沃斯论坛上表示,首批由AI设计的药物预计在2026年底进入临床试验。这家公司正从一个前沿科研机构,加速转变为一台高效的商业机器。
武田制药的计算结构生物学家Diego del Alamo指出了另一个微妙之处:Isomorphic Labs此前投入了大量精力与各大药企合作,很可能因此获得了大量未公开的私有实验数据。

这些额外的、高质量的私有数据对IsoDDE卓越性能的贡献有多大,外界无从知晓。如果其核心优势很大程度上构建在数据壁垒而非纯粹的算法创新之上,那么所谓的“激励”对开源社区而言,可能更像一种姿态。
开源阵营并未放弃,追赶与超越的竞赛开始
闭源引发了忧虑,但也点燃了竞争的火花。
Boltz-2的联合开发者、非营利组织Boltz的创始人Gabriele Corso态度明确。他认为,基于其团队观察到的进步,私有数据并非报告中所称性能的关键因素。“利用现有的公开数据,我们还有很多改进空间,”他表示,“我认为这是一个需要追赶的新基准——但也完全可以超越。”

另一家名为Deep Origin的公司更为高调。在IsoDDE发布次日,该公司便发布声明称,其自家的DODock引擎早在2025年8月就已在同一基准测试上达到了可比的性能水平——并且采用的是完全不同的技术路线。

事实上,开源社区在过去两年也并未懈怠。自AlphaFold 3发布以来,多个团队已经开发出性能接近甚至部分超越它的开源模型,例如Boltz-1/2、Chai-1、Protenix等。AI制药领域似乎正在重演大语言模型领域的剧本:一家公司展示惊艳的闭源成果,随后整个开源社区迅速跟进,将差距从“代际”缩小到“可以追赶”的距离。
但这里存在一个关键区别。大语言模型的训练数据——互联网上的海量文本,几乎是无限的公共资源。而AI制药所需的训练数据,特别是高质量的蛋白质-药物复合物实验数据,有相当一部分掌握在大型药企手中,并非完全公开可获。如果顶尖闭源模型的护城河是建立在私有数据之上,那么开源社区追赶的难度将大大增加。
反思:一扇正在关闭的门?
IsoDDE的发布及其闭源选择,其影响可能远超药物研发领域本身。
过去几年,“AI开源推动科学进步”是一个被广泛接受且令人振奋的叙事。AlphaFold正是这个叙事最有力、最成功的证据。每当人们质疑科技巨头的AI研究究竟惠及了谁时,AlphaFold及其数百万用户就是最好的回答。
如今,当AlphaFold的“直系后代”选择走上闭源道路,这个美好的叙事被撕开了一道口子。它暗示了一种可能的未来:AI在基础科学领域最强大的工具,正逐渐从全球科学家的“公共品”转变为公司的“商业资产”;突破性的成果更多以技术报告而非经同行评审的论文形式发布;学术界能看到令人惊叹的结果,却永远无法窥见其实现方法。
Hassabis曾说过,将AI应用于科学,是比开发语言模型“更丰富”的事业。这话没错,但“丰富”的前提是“开放”。当最强大的科学AI工具只对付费客户敞开,那么科学共同体中的绝大多数人,便只能站在围栏外观望。
AlphaFold的诺贝尔奖章上,镌刻着将知识赋予所有人的理想。IsoDDE的技术报告里,则描绘了一个更强大、但可能也更封闭的未来。两者之间的距离,正是我们这个时代在效率与开放、商业与公益之间所做出的选择。
对这一前沿动态感兴趣的朋友,可以到云栈社区的智能 & 数据 & 云板块,与更多开发者一起探讨AIGC与科学计算的未来。
参考资料:
- https://www.nature.com/articles/d41586-026-00365-7
- https://www.isomorphiclabs.com/articles/the-isomorphic-labs-drug-design-engine-unlocks-a-new-frontier
- https://storage.googleapis.com/isomorphiclabs-website-public-artifacts/isodde_technical_report.pdf