哺乳动物的大脑协调着信息的处理和整合,以指导行为,而意识状态的变化与此过程密切相关。为了刻画这种关联,近日,《自然·人类行为》期刊发表的一项研究以跨物种视角,尝试回答这一问题。研究团队结合功能磁共振成像数据和麻醉学方法,在人类、猕猴、狨猴和小鼠中开展研究发现,整合信息的崩溃是麻醉剂引发哺乳动物意识丧失的共同神经机制。进一步地,研究团队发现整合信息崩溃与PVALB/Pvalb基因表达的空间梯度模式相吻合。基于上述发现,研究团队开发了针对人类、猕猴和小鼠物种特异性的计算模型,证明了连接组和转录组梯度在控制大脑动力学和信息整合中各自的作用,为理解意识的神经基础以及开发意识障碍的治疗策略提供了新视角。
关键词:整合信息 (integrated information);麻醉 (anaesthetic);意识 (consciousness);连接组 (connectomics);转录组 (transcriptomics);PVALB / Pvalb ;中央丘脑 (centro-median thalamus);跨物种 (cross-species)

论文题目:Convergent transcriptomic and connectomic controllers of information integration and its anaesthetic breakdown across mammalian brains
论文链接:https://www.nature.com/articles/s41562-025-02381-5
论文来源:Nature Human Behaviour
长期以来,神经科学面临一个悖论:尽管各式各样的麻醉药物——从作用于γ-氨基丁酸 (GABA) 受体的丙泊酚,到通过NMDA通道阻滞作用的氯胺酮,再到挥发性麻醉剂七氟醚——在分子层面的作用完全不同,但它们都会让哺乳动物失去意识与对环境的反应能力。这一悖论是否暗示了这些麻醉药物的效应共同作用在宏观尺度的大脑活动?如果是的话,这一宏观尺度的大脑活动可能是什么?本研究以跨物种视角,不仅发现了不同麻醉剂作用下哺乳动物大脑意识状态变化的共同宏观表征——整合信息能力,而且揭示了背后的分子生物学机制。
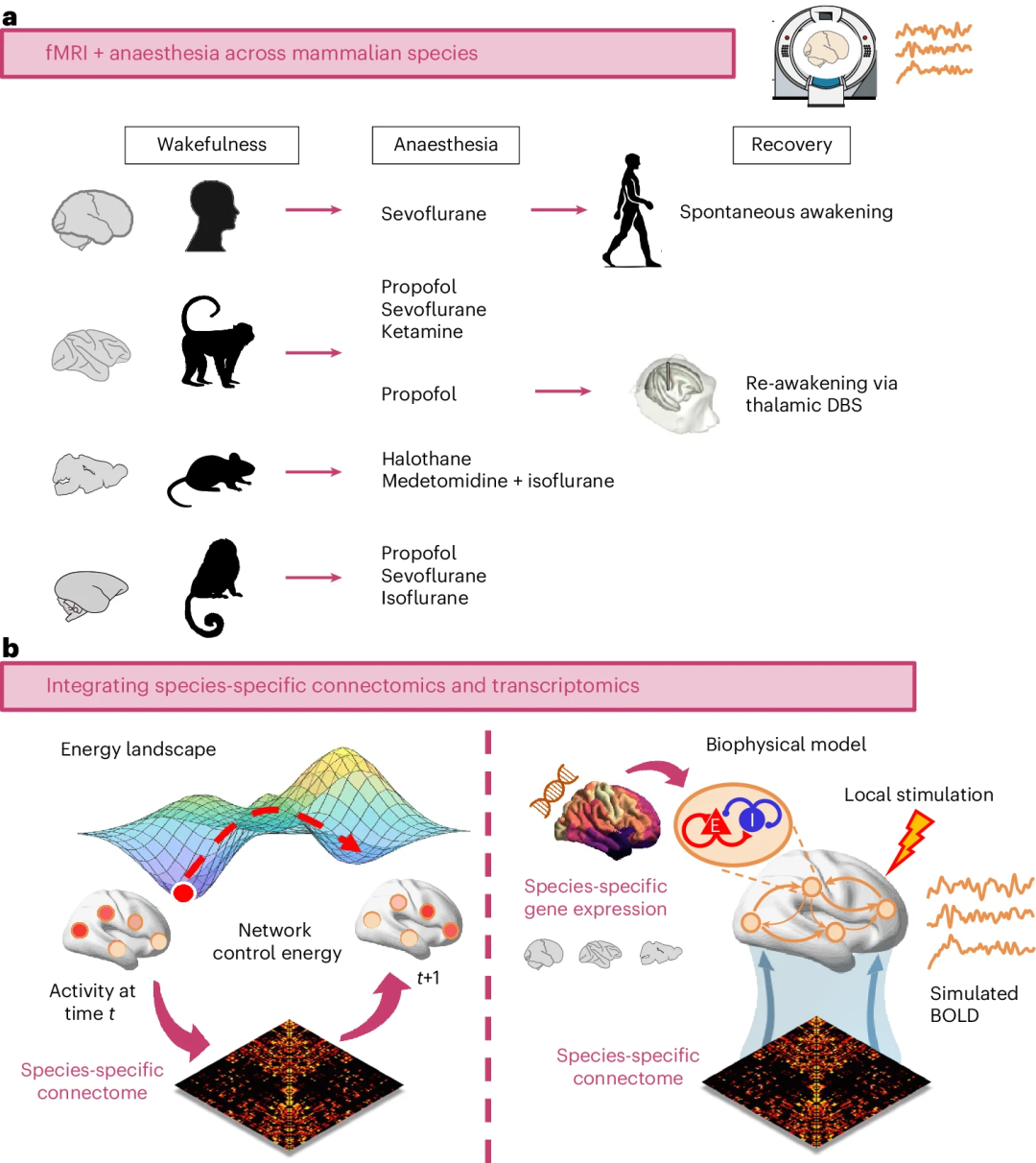
图1:a. 采集四种哺乳动物(人类、猕猴、小鼠和狨猴)在清醒状态和多种麻醉方案(七氟烷、丙泊酚、氯胺酮、异氟烷、氟烷和异氟烷-美托咪定)下的功能磁共振成像 (fMRI),人类的自发意识恢复过程以及猕猴在持续麻醉输注期间通过丘脑深部脑刺激 (DBS) 诱导的意识恢复过程中的fMRI,基于fMRI数据计算整合信息能力的变化;b. 运用网络控制理论和生物物理计算模型,通过整合人类、猕猴和小鼠的物种特异性结构连接和物种特异性基因表达,提供机制方面的见解。
意识与整合信息 $\Phi_R$
麻醉效应与信息整合能力紧密相关。研究团队基于部分信息分解 (partial information decomposition, PID) 框架,定义整合信息 $\Phi_R$ (integrated information) 作为衡量的是大脑跨区域地整合来自不同脑区信息的能力。基于四个物种在多种麻醉状态下的功能连接计算对应的$\Phi_R$。发现无论使用七氟醚 (Sevo)、丙泊酚 (Ppfl)、氯胺酮 (Keta)、美托咪定-异氟烷 (MedIso) 还是氟烷 (Halo),无论扫描对象是人类、猕猴、狨猴还是小鼠,麻醉都显著降低了大脑的整合信息。这种效应在深度麻醉时最为明显,而当麻醉停止、人类受试者恢复意识后,信息整合能力也随之回升。
整合信息是麻醉的伴随现象吗?研究者进一步对猕猴开展了神经调控实验:在丙泊酚连续输注的情况下,实施中央丘脑 (centro-median thalamus) 电刺激,成功使其从麻醉状态恢复了行为反应能力,此时大脑的整合信息能力$\Phi_R$也显著回升。相比之下,对腹外侧丘脑 (ventrolateral thalamus) 的刺激则没有这种效果。并且,$\Phi_R$比因果密度、信息流等其他意识相关指标能更好的预测猕猴的行为唤醒水平。这一实验不仅说明了中央丘脑作为全脑的动力学控制枢纽,通过控制整合信息控制大脑的意识状态。
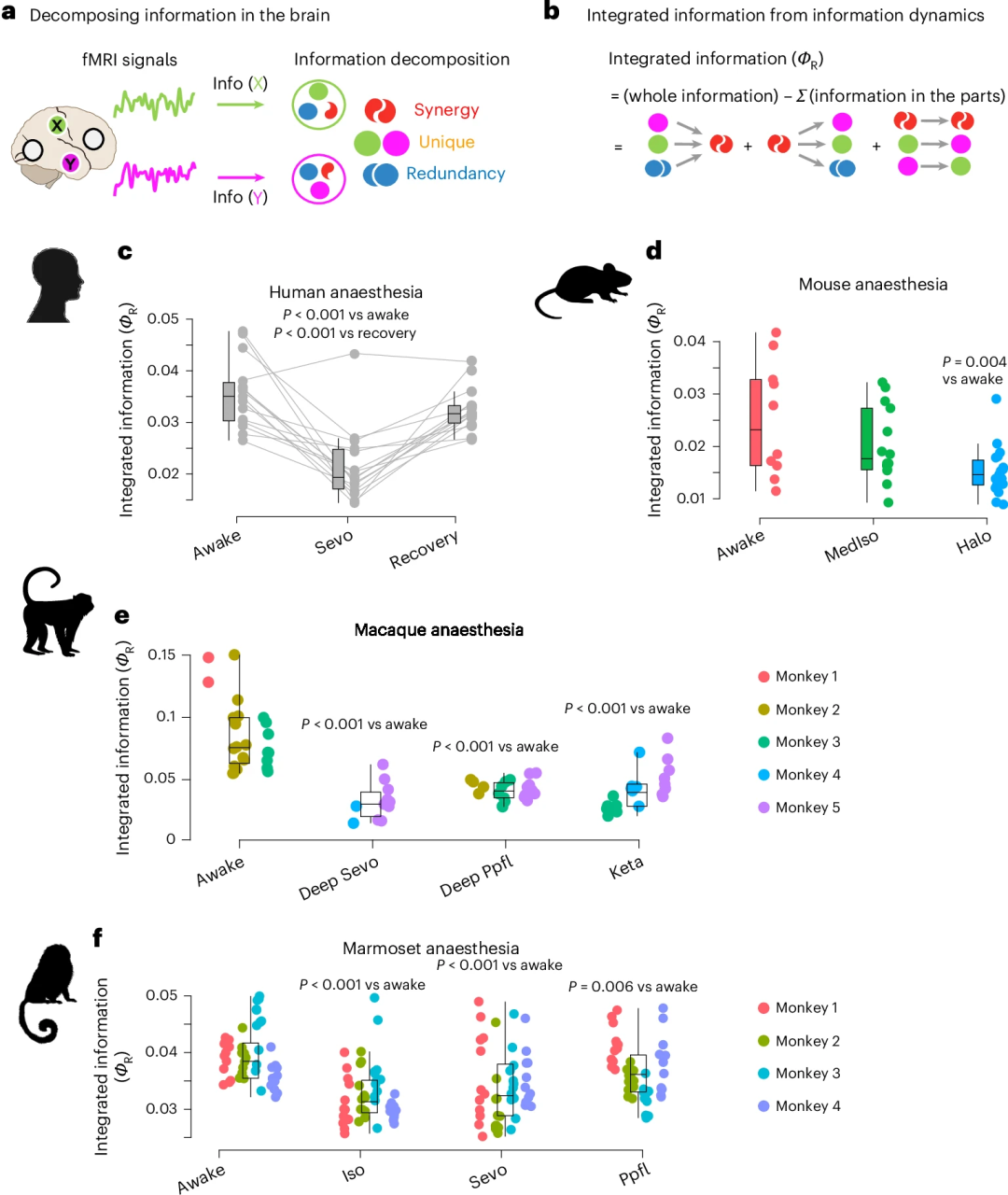
图2: a. 两个变量 X 和 Y (脑区)共同携带的总信息可以完全分解为:冗余信息 (Redundancy);独特信息 (Unique);协同信息 (Synergy),三种信息随时间的演化产生信息的动力学;b. 整合信息$\Phi_R$反映系统各组成部分之间相互作用的信息动力学[1];c. 人类麻醉 (Sevo) 与清醒状态与麻醉后恢复状态 n = 15的比较;d. 小鼠清醒状态 ( n = 10) 与不同麻醉剂 (MedIso; n = 14,Halo; n = 19) 麻醉状态与清醒状态的比较。e. 猕猴清醒状态(3只动物共24次实验)与使用不同麻醉剂(Ppfl,3 只动物共23 次实验、Sevo,2只动物共11次实验、Keta,3 只动物 共22 次实验) 麻醉状态的比较。f. 狨猴清醒状态与使用不同麻醉剂 (Iso、Sevo、 Ppfl)麻醉的比较,每种麻醉条件下,4 只动物共 48 次实验。P 值来自线性混合效应模型(双侧),并经 FDR 校正以进行与清醒状态的多重比较。 所有箱线图:中心线代表中位数;箱体上下限分别代表上四分位数和下四分位数;须线代表 1.5 倍四分位距。相同颜色的数据点代表同一动物。
整合信息 $\Phi_R$ 的分子基础
整合信息与中央丘脑之间的对应关系是否能找到分子层面的证据?利用艾伦脑科学研究所提供的人类和小鼠转录组数据库,以及中国科学院最新发布的猕猴皮层单细胞空间转录组数据,研究者筛选了81个进化保守的脑相关基因,考察其表达模式与麻醉下整合信息下降的空间相关性。在所有基因中,相关性最稳定、最一致的,是 PVALB / Pvalb 基因。
PVALB / Pvalb 编码的是一种名为小清蛋白的钙结合蛋白,它是特定类型抑制性中间神经元——PV+神经元的标志物。这些神经元在大脑中扮演着“节拍器”的角色,控制着神经环路的放电时机和同步性,也正是许多麻醉药物作用的靶点。并且在所有三个物种中,PVALB / Pvalb 表达水平与整合信息的下降的空间模式呈现显著的负相关。
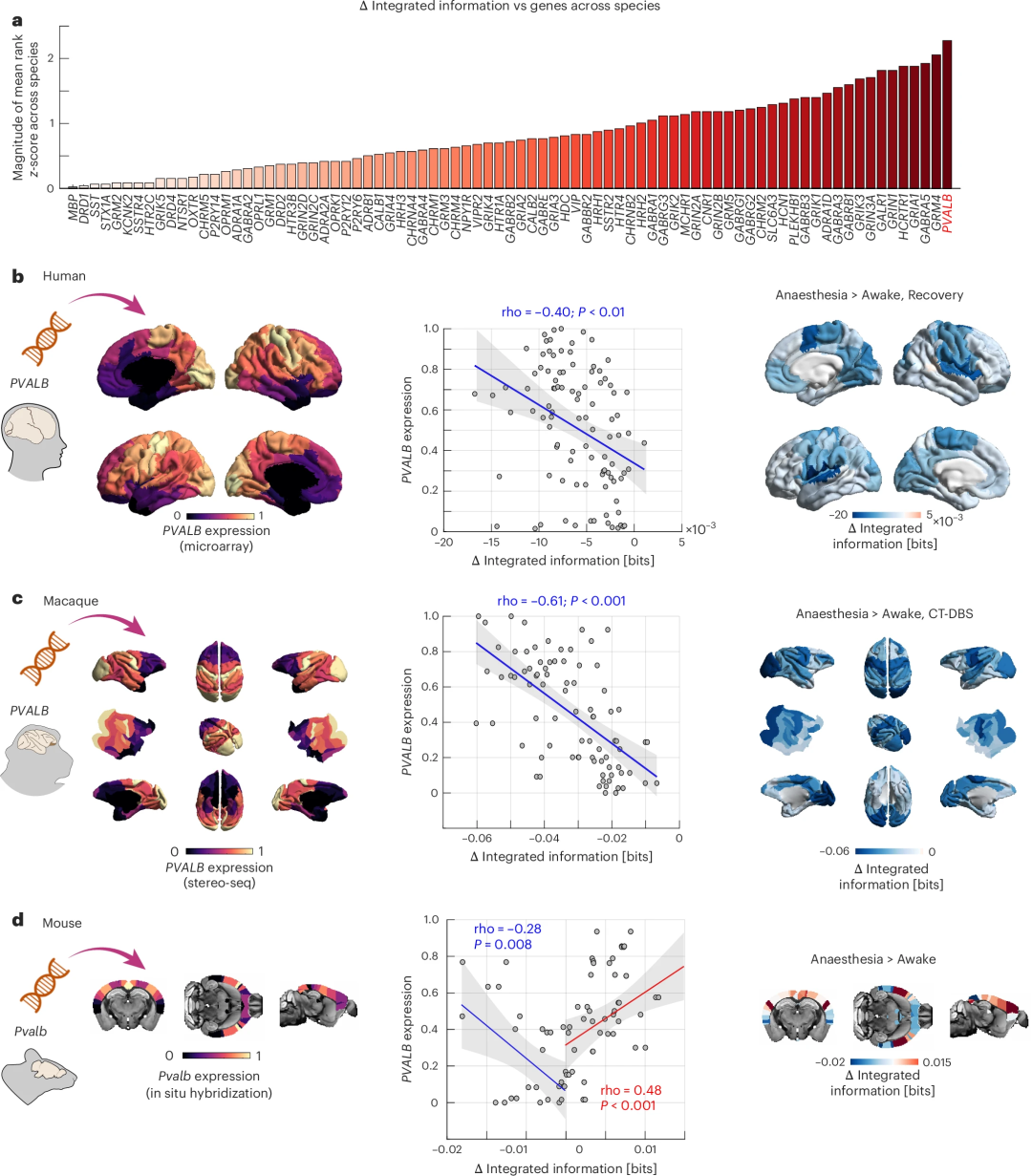
图3 a. PVALB / Pvalb 基因与整合信息的空间关联在不同物种间最为一致。使用空间相关性比较每个物种内的 81 个基因,对三个物种的排名取平均值并归一化 (z-score) 处理,并按相关性从负到正进行排序;b. 从艾伦脑科学研究所 (AIBS) 转录组数据库获取了人脑区域定义的 PVALB 基因表达数据。观察到 PVALB 基因表达的皮层分布与整合信息显著降低之间存在负空间相关性,整合信息显著降低值是通过比较麻醉与基线和恢复期得到的;c. 从中国科学院脑科学数据中心提供了猕猴脑区域定义的 PVALB 基因表达数据,观察到 PVALB 基因表达的皮层分布与整合信息显著降低的平均值之间存在负空间相关性;d. 小鼠脑的区域性 Pvalb 基因表达数据来自 AIBS 转录组学数据库,观察到 Pvalb 基因表达的皮层分布与整合信息显著降低的平均值之间存在负空间相关性。在浅麻醉状态下整合信息增加的区域,我们观察到皮层中 Pvalb 基因表达的分布与整合信息显著增加值之间存在正向空间相关性。[人与猕猴的数据是在深度麻醉下采集的,目的是为了彻底抑制行为反应。而小鼠的数据(特别是用“右美托咪定-异氟烷”组合的那一组),目的是让小鼠在尽可能“接近清醒”的状态下保持不动,所以整合信息显著增加并且与 Pvalb 基因表达呈正相关]
从相关到因果:计算模型的洞见
为了进一步验证 PVALB / Pvalb 是否真的能够调控整合信息,研究者构建了针对人类、猕猴和小鼠的全脑生物物理模型——动态平均场模型。每个模型都基于该物种真实的结构连接组,并经过调参以复现清醒状态下的功能连接动态。他们根据每个脑区 PVALB / Pvalb 的表达水平,在模型中增加该区域的抑制性输入。结果发现,这种基于转录组的异质性抑制,显著降低了模拟脑活动的整合信息能力。而采用随机生成但保持空间自相关的对照图谱则没有这种效应。
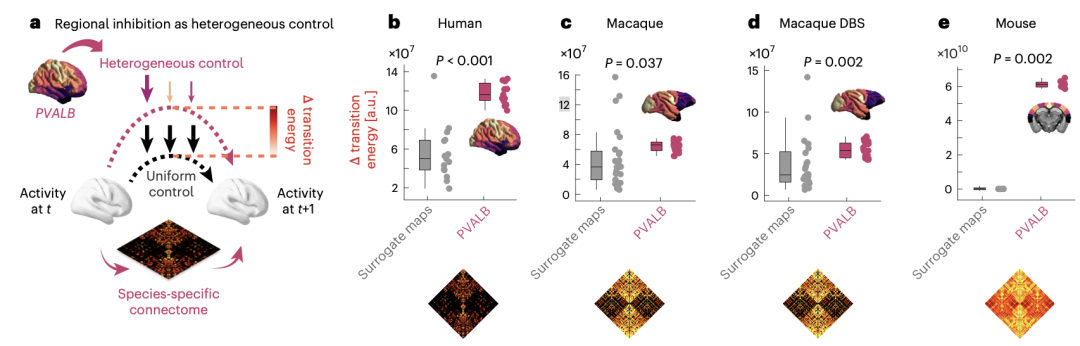
图4 a. 将区域异质性抑制建模为每个区域可注入系统的抑制能量的减少量,该减少量与该区域的 PVALB / Pvalb 表达量成正比。b-e. 在每个数据集中,将 PVALB / Pvalb 表达导致的抑制成本增加与保留空间自相关但打破PVALB / Pvalb分布的抑制成本增加进行比较,结果表明,由于 PVALB / Pvalb 的解剖分布,其导致的转换成本显著增加。人类: n = 15;猕猴: n = 24,来自 3 只动物;猕猴 DBS: n = 36,来自 3 只动物;小鼠: n = 10。
研究者还构建了一个包含丘脑-皮层连接的猕猴模型。在这个模型中,他们模拟了对中央丘脑和腹外侧丘脑的电刺激。结果表明只有刺激中央丘脑,才能显著恢复麻醉模型的整合信息,而且刺激强度越高,效果越明显。由于模型中两个丘脑核团的唯一区别在于它们与皮层的解剖连接模式,这个结果有力地说明,中央丘脑之所以能够成为唤醒的“开关”,很大程度上归功于其独特的连接组结构。
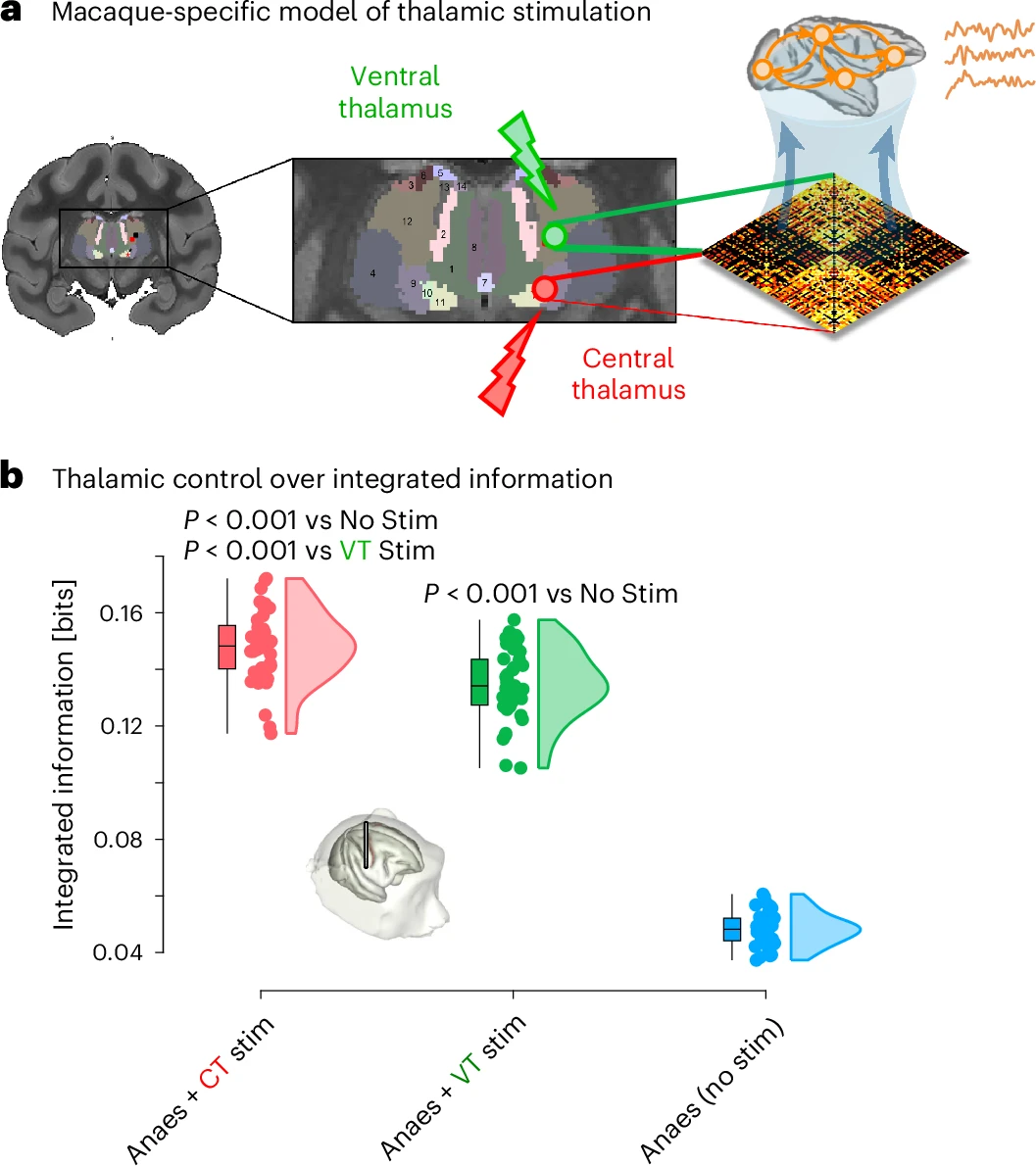
图5 包含丘脑-皮层连接的猕猴模型。a. 丘脑感兴趣区域及其在模型中的应用示意图;b. 模拟中央丘脑刺激在脑动力学中实现了显著的整合信息,优于无刺激。
迈向“整合”的未来
当我们谈论意识时,我们谈论的究竟是什么?这项研究给出了一个可能的答案:意识,或许就是大脑整合各部分信息的能力。而这种能力,深深地根植于基因组、连接组,以及进化之中。
这项研究不仅仅是描述了实验现象,而是构建了一个从基因组到连接组、再到全脑动力学的完整框架。它告诉我们,进化保守的 PVALB / Pvalb 基因表达梯度,塑造了皮层不同区域对麻醉的敏感性;而中央丘脑独特的连接模式,则使其成为调控全局整合信息的枢纽。
当然,研究也存在局限性。信息分解的计算复杂度限制了目前只能分析成对脑区,而更高阶的相互作用可能更为关键。小鼠与灵长类在麻醉深度上的差异,也使得某些结果未能完美对齐。但这项研究为意识科学提供了一套强大的方法论框架,并指向了潜在的临床应用。研究者构建的丘脑刺激模型,理论上可以用于筛选其他可能更优的刺激靶点,或为意识障碍患者制定个性化的神经调控方案。
参考文献
- Mediano, P. A. M. et al. Toward a unified taxonomy of information dynamics via Integrated Information Decomposition. Proc. Natl. Acad. Sci. USA 122, e2423297122 (2025)
本文解读了一项融合了功能磁共振成像、单细胞空间转录组分析和网络控制理论的复杂科学研究。对前沿脑科学和计算模型感兴趣的朋友,欢迎在云栈社区交流探讨。