说到通过饮食改善肠道健康,以往的建议常常很笼统,比如“多吃蔬菜水果”。这听起来没错,但正因为过于正确,反而缺乏具体的指导价值。
最近,《自然》子刊《自然-医学》(Nature Medicine)上发布了一项大规模研究,为我们提供了更细致的洞见。基于对上万名参与者数据的分析,这项研究发现,爱吃肉并不总是破坏肠道平衡,而仅仅调整餐桌上的几样食物,就可能带来显著的代谢益处[1]。

你的餐桌,正在喂养怎样的菌群?
这项研究分析了超过1万名个体的详细饮食记录与肠道菌群数据。在控制了年龄、性别、体重等混杂因素后,研究人员利用算法模型,系统性地评估了我们日常摄入的食物以及遵循的饮食模式,与肠道微生物组成及功能之间的关联。
话不多说,直接来看核心发现:
发现一:维护菌群多样性,关键在于拒绝过度加工
肠道菌群的多样性通常被视为肠道生态系统健康与稳定的重要标志。更高的多样性往往意味着更强的抵抗力和更低的慢性炎症风险,这与对抗衰老密切相关。
研究证实,饮食确实能显著影响肠道菌群的多样性,但其解释力约占6-7%。在众多饮食因素中,食物的加工程度是最关键的决定性变量:无论是植物还是动物来源,摄入更多未加工或最低限度加工的食物,都能有效增加菌群多样性。相反,超加工食品(如精制面包、糕点)则会明显降低多样性。
这一结论在饮食模式分析中得到呼应:以天然、高营养密度为特点的健康饮食模式(如替代健康饮食指数,AHEI) 最有利于提升多样性。而一个有些反直觉的发现是,以动物性食物为主的饮食模式,也与较高的菌群多样性相关,其效果与AHEI模式相当。这提示我们,单纯的“荤素”二分法可能过于简单,食物的质量和加工方式或许更为关键。
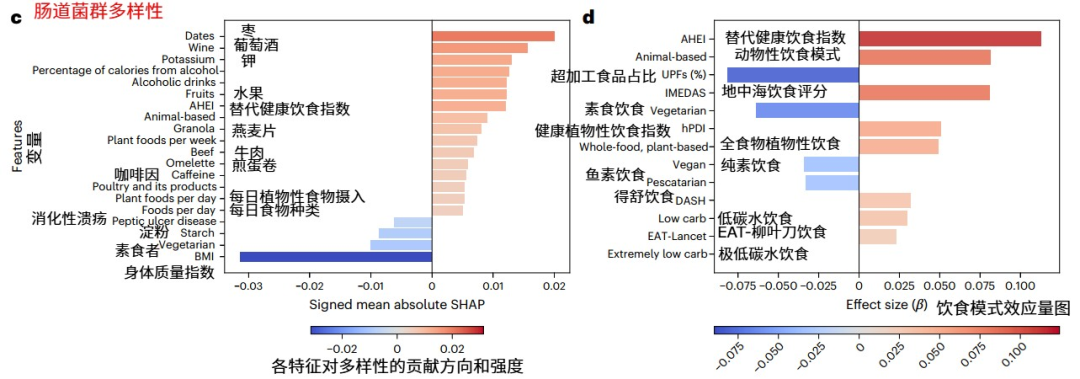
图注:食物特征和不同饮食模式对肠道菌群多样性的影响。左侧(c)显示各特征对多样性的贡献强度,右侧(d)比较不同饮食模式的效应量。
发现二:咖啡、酸奶、坚果,各自“偏爱”不同的细菌
研究进一步发现,特定的食物与肠道内某些细菌的相对丰度存在显著关联。这为我们“喂养”有益菌提供了更精确的线索:
- 咖啡的摄入与产丁酸菌——解糖劳森氏菌(Lawsonibacter saccharolyticus)的增加相关。
- 酸奶和牛奶分别与益生菌嗜热链球菌(Streptococcus thermophilus)和长双歧杆菌(Bifidobacterium longum)的丰度升高有关。
- 坚果的摄入则与一种可能参与血脂调控的细菌(UBA11774 sp003507655)相关联。
- 香蕉与可能参与碳水化合物发酵的梭菌(Clostridium sp900539375)增加相关。
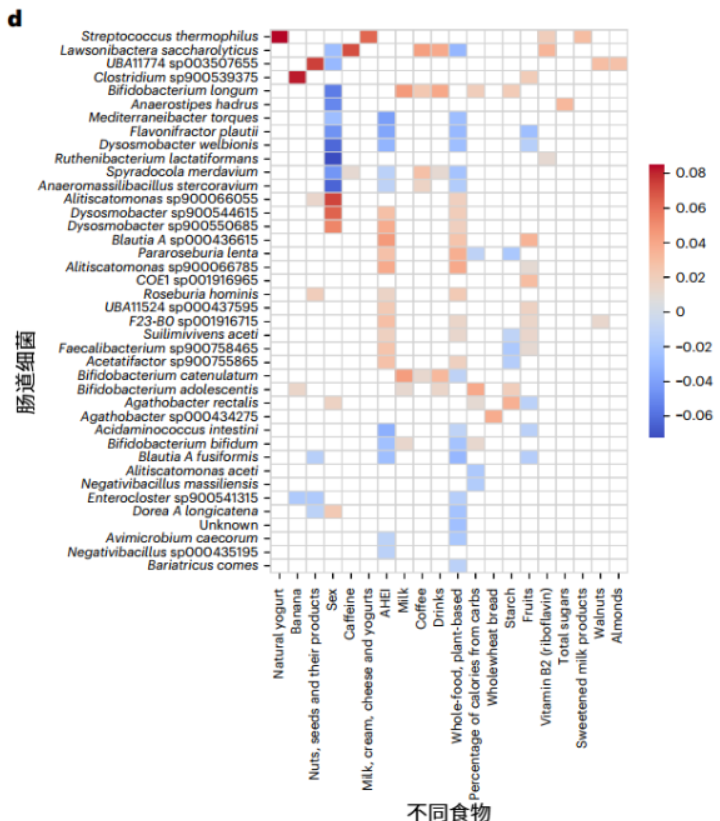
图注:热图展示了不同食物与多种肠道细菌相对丰度之间的统计学关联(红色为正相关,蓝色为负相关)。
从宏观的饮食模式来看,不同的饮食风格整体上塑造了截然不同的肠道菌群生态结构。例如,健康的天然食物模式(AHEI)、允许部分动物制品的植物性模式(如鱼素、纯素)以及动物性为主的低碳模式,都对应着独特的微生物群落构成。这意味着,一个人长期的饮食习惯,正在默默勾勒其独特的肠道微生物“风景画”。
图注:咖啡可能通过其多酚等成分,发挥益生元效应,间接促进特定有益菌的生长。
发现三:饮食塑造菌群的功能“技能树”
除了改变菌群成员,饮食还深刻影响着它们的“工作内容”。研究发现,以天然、未加工、富含植物性食物为特点的饮食模式,倾向于让肠道菌群合成更多对人体有益的代谢分子,例如多种氨基酸和核苷酸。
同时,肠道菌群也会根据主人的饮食习惯,调整其营养代谢的“专业技能”。比如,水果摄入量高的人群,其肠道菌群整体表现出更强的果胶及相关糖类降解能力;而乳制品和咖啡(常与牛奶同饮)摄入多的人,他们的菌群则更擅长分解乳糖。
这些关联在不同的人群队列和长期随访数据中都得到了验证,凸显了饮食与肠道菌群之间稳定而强大的联系。这项研究运用了大规模的数据分析技术,揭示了复杂生物系统中的规律,这正体现了大数据研究在生命科学领域的价值。
从关联到预测:个性化饮食模拟模型登场
既然发现了强关联,研究便向前推进了一步。团队开发了一套 “个性化饮食模拟模型” ,旨在预测:当一个人改变饮食时,其肠道菌群和关键健康指标(特别是心血管代谢指标)将如何响应。
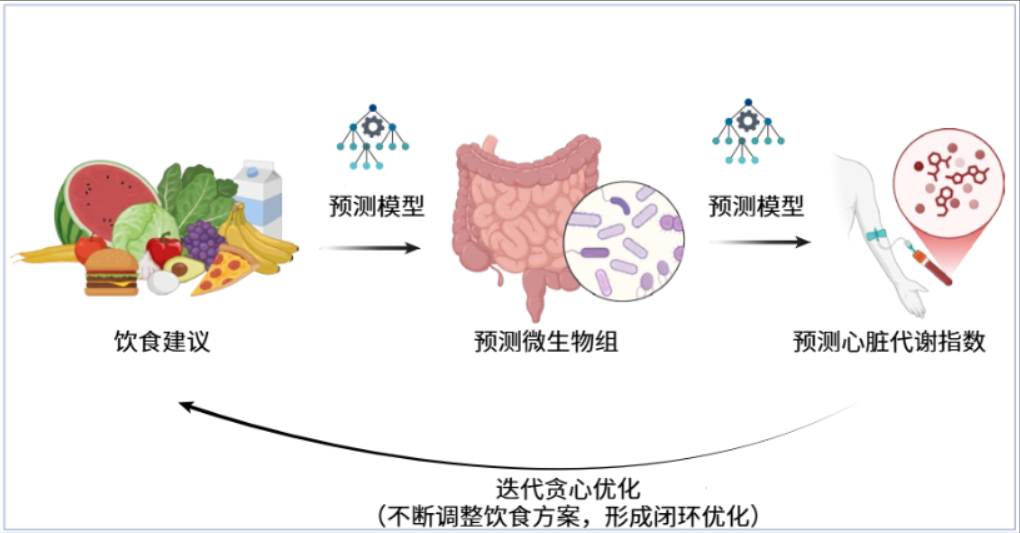
图注:个性化饮食模拟模型工作流程:基于饮食建议,通过预测模型预估微生物组变化,进而预测心脏代谢指数,并形成闭环优化。
研究首先确认了一个关键前提:食物对健康的影响,很大程度上是通过肠道菌群这一媒介实现的。基于此,模型有望为个体提供定制化的饮食建议。
在2000多人的预测案例中,我们以一位五六十岁的男性为例。模型分析其现有饮食后,给出了一个具体且微调的建议:减少白面包的摄入,增加苹果和卷心菜的食用量。
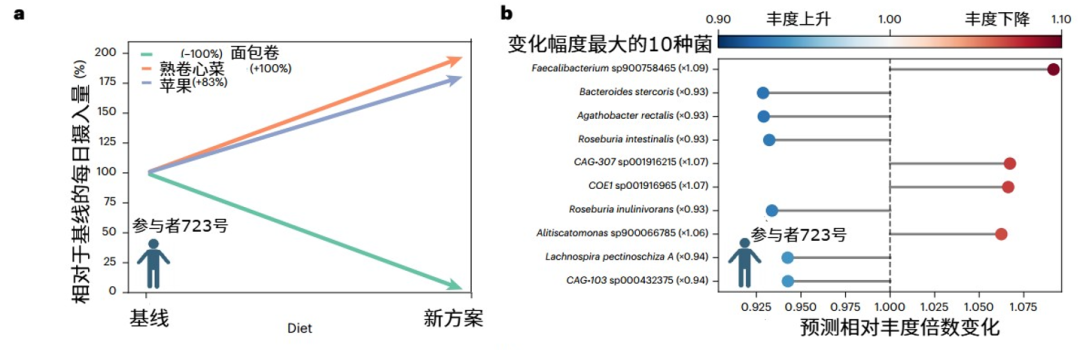
图注:参与者示例。图a显示调整前后三种食物的摄入量变化;图b显示预测中变化最大的10种细菌及其丰度变化倍数。
模型推演显示,遵循此建议后,该个体的肠道菌群会向更健康的方向转变,同时一些不良的心血管代谢指标也呈现下降趋势。
在整个预测人群中,模型建议的饮食调整(通常只涉及少数几种食物,且总热量变化不大)普遍显示出对肠道菌群和心血管代谢指标的改善趋势。 这表明,即使是小幅、精准的饮食调整,也可能通过肠道菌群的“放大”作用,带来可观的健康收益。这种基于模型的预测与优化,正是人工智能和算法在健康管理领域的前沿应用探索。
精准营养时代:已来的未来
通过饮食进行个性化健康干预,正从概念走向实践。美国国立卫生研究院(NIH) 已启动名为 “精准营养研究” 的大规模项目,计划招募万名参与者,综合考察基因、肠道菌群、生活方式等多维度因素,旨在彻底改变“一刀切”的饮食指南,迈向真正的个性化营养[2,3]。
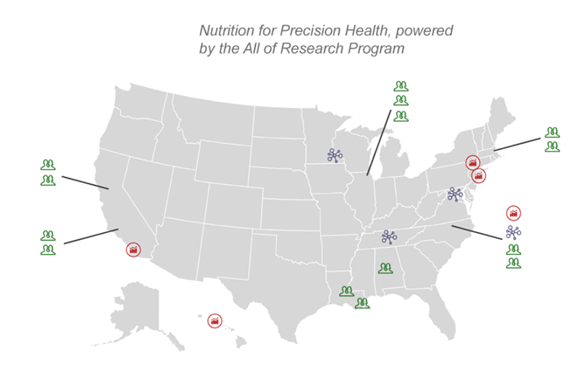
图注:美国“精准营养研究”项目在全美的研究站点分布示意图。
与此同时,临床探索和商业应用也已展开:
- 2024年一项小规模临床研究报道,基于个体肠道菌群检测定制的个性化饮食方案,在短期内改善2型糖尿病合并高脂血症患者的相关指标方面,可能优于传统的标准饮食建议[4]。
- 英国数字健康公司ZOE是商业化应用的例子。它通过整合用户的肠道菌群数据、血糖反应等多维信息,提供个性化的食物评分和饮食建议[5]。

图注:ZOE类应用通过拍照识别食物,并结合用户个人数据提供实时营养评分。
这些尝试正在将前沿科研成果转化为可触达的健康服务。然而,我们必须清醒认识到,人类对肠道微生物世界的了解仍非常有限。正如一位进化生物学家所言:“这有点像你砍掉了一平方英尺的树叶,吸进吸尘器带走,然后回来说你了解了雨林”[6]。
尽管如此,通过科学饮食来滋养肠道菌群,进而促进长期健康,这个大方向无疑是正确的。这项基于万人数据的研究,至少为我们提供了一些更精细的“喂养”线索:关注食物加工度、重视天然食物多样性,并理解咖啡、酸奶、坚果等具体食物与菌群的特殊“对话”。在追求健康的道路上,我们或许可以更聪明地运用自己的“主观能动性”,而不仅仅是听从笼统的建议。对这类融合了生命科学与数据技术的交叉领域话题感兴趣?欢迎来云栈社区的智能 & 数据 & 云板块,与更多同行交流探讨。
参考文献
[1] Segev, T., Barak, D., Zahavi, L., Godneva, A., Rein, M., Krongauz, D., Samocha-Bonet, D., Rossman, H., Weinberger, A., & Segal, E. (2026). Diet-microbiome associations in 10,068 individuals from the Human Phenotype Project to guide personalized nutrition. Nature medicine. Advance online publication.
[2] https://allofus.nih.gov/article/announcement-nih-launches-largest-precision-nutrition-research-effort-its-kind
[3] https://nutritionforprecisionhealth.org/
[4] Kallapura, G., Prakash, A. S., Sankaran, K., Manjappa, P., Chaudhary, P., Ambhore, S., & Dhar, D. (2024). Microbiota based personalized nutrition improves hyperglycaemia and hypertension parameters and reduces inflammation: a prospective, open label, controlled, randomized, comparative, proof of concept study. PeerJ, 12, e17583.
[5] https://zoe.com/how-it-works
[6] https://www.wired.com/story/gut-health-personalized-nutrition/